据telegraph报道:2024年1月,卡里姆·布亚赫里坎 (Karim Bouyakhrichan)在西班牙城市马贝拉遭到逮捕。听到这个消息,荷兰王室长长地松了一口气。能得到王室的关注,这个卡里姆 …
阅读更多 »-
加拿大夫妇疑似拍到尼斯湖水怪照片!全球疯传:令人信服的新证据
据CBC报道:本月早些时候,移居英国的加拿大夫妇帕里·马尔姆(Parry Malm)和香农·怀斯曼(Shannon Wiseman)带着2个孩子前往苏格兰尼斯湖游玩时,竟意外拍摄到了疑似尼斯湖水怪的照 …
阅读更多 » -
惊曝!最臭名昭著连环杀手竟可申请“日间假释”!大温12位市长紧急联名上书
-
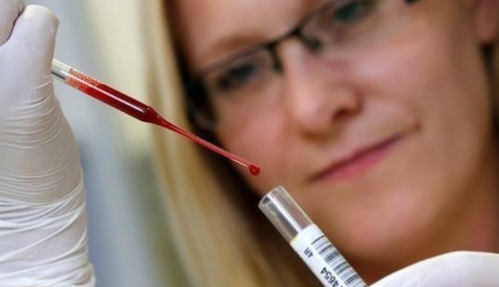
“AI救了我的命”! 加拿大女子被AI提前诊断致命癌症! 去医院一查惊了
-
加拿大贫富差距拉大!中产正在失去动力
-
惨!大温著名景点惊爆连环砍人!受害者刚到加拿大 是家中顶梁柱!
-
刚刚!加拿大发布旅行建议:谨慎前往8个国家和地区!包含热门度假地!
-
联邦政府“通吃”全加拿大人!低收入“边际有效税率”高达50%!
-
不装了!零元购白天冲进店铺打砸抢;女子当街被劫车 特斯拉报废
-
惹众怒! 年薪10万加拿大小哥狂薅救济食物, 每月省几百! 结果悲剧了
-
大温华人遭暴力破门盗窃!门锁被撬坏、珠宝摄像头被盗,但警察竟然这样说…..
据City News报道:和家人在外面吃完晚饭回到家,却发现有人在他们之前使用暴力破门而入。原本家是最安全的地方,但是Alice Lin和家人却不敢再住这里:“窃贼偷走了一些珠宝和摄像头,但是这与事件 …
阅读更多 » -
丢人!华人男子从国内偷运这东西到加拿大卖!被抓现行重罚$35000!
-
恐怖! 亚裔男为独吞退休金 刀捅活埋妻子12小时 惊骇细节曝光!
-
全网炸了!加拿大华人移民泪诉:37岁妻子确诊13天,被执行“安乐死”!
-
加拿大华人绑架中国富二代! 下药+拴铁链囚禁 要550万赎金 装追踪器复制钥匙
-
移民太难!加拿大过万留学生申请当难民!多大今年限招6200,滑铁卢更少
-
中国女游客网红景点拍照, 被裙子绊倒坠崖身亡! 丈夫悲痛欲绝…
-
网红华裔小哥对比美加两国Costco食品价格:有一些惊人的发现!
-
多名华人被捕!“红钩行动”严打这些犯罪!大批加拿大华人遭殃!
-
惊呆! 女子携10瓶茅台入境, 竟躲卫生间6小时! 还有人带316个LV包
据温哥华港湾综合报道:真是惊呆了!据广州边检,近日,广州边检总站白云边检站民警在执行某入境航班边防检查任务时面对着数据却陷入了沉思….因为实际验放量与载客数总是对不上,1名旅客在下机2个小 …
阅读更多 » -
“撞死你也就20万的事” 保时捷女司机撞车后恐吓对方 警方通报来了!
-
火遍全网!华人妹子回国逛Costco!加拿大人羡慕哭了!
-
南大拒绝录取考研第1名的残忍虐猫者!调剂到兰大疑似也未通过面试?!
-
蛇蝎骗婚女翟欣欣疑认罪或将判10年?致命毒妻行径更甚:骗30个男友上亿,手握多条人命!
-
汪小菲警局怒告前妻!身穿“破烂抹布”!4500名牌穿出4.5包邮既视感!
-
河北3名初中男生霸凌杀害同学埋尸!家人拒道歉玩消失?
-
网上炸了!百亿富豪、中国巴菲特、创投教父都已移居新加坡?
-
与7000多名女性私密聊天记录曝光! 这个洋垃圾的真实面目, 令人作呕…
-
震惊!加拿大华人业主仅离开豪宅3个月,回来家中已住满陌生人…
据多伦多都市网综合报道:在社交媒体上搜索“加拿大”+“入室”或“break-in”等关键词就会搜索出各种令人惊心动魄的图——被杂碎的玻璃、摊开的行李箱以及飓风席卷过般的厨房…最近,多伦多出 …
阅读更多 » -
加拿大女子被迫卖房! 花2倍房贷租房住; 华女狠人吃米饭+辣椒酱存钱 买6套房
-
BC省长发狠!5月1日起实施新规:房东违规一次最高罚$5000
-
出手了!加拿大CRA严查6大税务!侧重房产交易和海外资产: 大批华人受影响!
-
判了!中文购房合同在加拿大有效!大温华人房主获赔40万…
-
最新! 大温楼花预售火爆 本月预计将上市2000套! BC房价增长6.5%
-
抛弃特鲁多!加拿大房价今年涨幅远超年初预测,年轻人彻底绝望
-
CRA这是抢钱?!房东未缴税,租客却惨了!这项规定99.99%的租客并不知道…..
-
噩梦!加拿大一大批房主搬新家,结果天天吃土,厕所“地震”一样!卖掉巨亏
 加国热点-itop366.com 加拿大新闻,温哥华新闻,多伦多新闻,蒙特利尔新闻,加国新闻,加国热点,加拿大热点
加国热点-itop366.com 加拿大新闻,温哥华新闻,多伦多新闻,蒙特利尔新闻,加国新闻,加国热点,加拿大热点